مقدمه
کروماتوگرافی مایع با کارایی بالا (High Performance Liquid Chromatography) یا HPLC مهمترین و متداولترین روش کروماتوگرافی است که کاربرد گستردهای برای محدوده وسیعی از مواد غیر فرار دارد. این روش در اوایل قرن بیستم کشف شد و برای اولین بار به منظور جدا کردن ترکیبات رنگی مورد استفاده قرار گرفت. مخترع این روش، گیاهشناس روسی میخاییل تسوت (Mikhail Tsvet) بود که برای مطالعه رنگ برگها از آن بهره گرفت.
HPLC روشی برای جدا کردن اجزاء یک مخلوط، شناسایی و اندازهگیری اجزاء آن است. این جدایش بر اساس برهمکنش نمونه با فاز ساکن جامد (ستون) و فاز متحرک مایع (حلال) انجام میشود. این روش بر اساس قطبیت فاز ساکن به دو دسته فاز نرمال (فاز ساکن قطبی) و فاز معکوس (فاز ساکن غیرقطبی) و بر اساس روش جداسازی به انواع جذب سطحی، تعویض یون و طرد اندازه تقسیمبندی میشود. HPLC را میتوان نوع پیشرفته کروماتوگرافی مایع با بازده، سرعت و کارایی بیشتر دانست.
شمای کلی از کروماتوگرافی مایع
اجزاء یک مخلوط، بر اساس تمایل هر جزء به فاز مایع، در ستون، جداسازی میشوند. بنابراین، اگر قطبیت اجزاء متفاوت باشد و فاز ساکن با قطبیت شدید از میان ستون عبور کند، یکی از اجزا با سرعت بیشتری (نسبت به بقیه) از داخل ستون عبور خواهد کرد. از آنجایی که مولکولهای یک ترکیب، به صورت گروهی حرکت میکنند، ترکیبات به صورت باندهایی جداگانه و مشخص در ستون از یکدیگر متمایز هستند. اگر اجزاء جدا شونده، رنگی باشند، در زمان کروماتوگرافی، باندهای رنگی متناظر با هر گروه قابل تشخیص خواهند بود. در غیر این صورت، همچون HPLC، حضور باندهای متناظر هر گروه را به کمک سایر روشها مانند طیفسنجی ماورابنفش- مرئی شناسایی میکنند.
نحوه جداسازی اجزاء در کروماتوگرافی مایع
در یک مخلوط دو جزئی با عبور فاز ساکن از میان ستون، هر دو جزء به صورت باندهایی مجزا از یکدیگر جدا میشوند. زمانی که هر جزء از ستون، شویش شود، هر کدام را میتوان بسته به نوع روش مورد نظر، جداسازی و بررسی کرد. بر اساس نوع قطبیت فازهای ساکن و متحرک، قطبیتهای نسبی هر دو جزء قابل تعیین است.
آمادهسازی ستون کروماتوگرافی مایع
فاز ساکن در کروماتوگرافی ستونی (Column Chromatography)، به طور معمول، یک جاذب جامد است. این جامد میتواند اجزاء مایع و گازی را در سطح خارجی خود حفظ کند. ستونی که به طور معمول در کروماتوگرافی ستونی از آن بهره میگیرند همانند پیپت پاستور است که در کروماتوگرافی ستونی با مقیاس پایین مورد استفاده قرار میگیرد. بخش نازک خروجی را با پشم شیشه یا صفحهای متخلخل پر می کنند تا مواد پرشده داخل ستون را حفظ کند. در ادامه، جامد جاذب (به طور معمول سیلیکا) را به صورت فشرده به داخل لوله شیشهای میفرستند تا ستون را تکمیل کند. پر کردن ستون با فاز ساکن باید با دقت کافی انجام شود تا توزیع یکنواختی از مواد در داخل ستون صورت بگیرد.
این توزیع یکنواخت برای جلوگیری از ایجاد حباب یا کانالیشدن در ستون انجام میشود. در انتهای آمادهسازی ستون، حلال مورد استفاده در فاز متحرک را از میان ستون خشک عبور میدهند. چنین ستونی را تَرشده (Wetted) مینامند. زمانی که ستون، به خوبی آماده شد، نمونه را در بالای ستون قرار میدهند.
اساس کار HPLC
اجزاء مولکولی در HPLC، دو دسته مهم را به نام آنالیت و ماتریکس تشکیل میدهند. آنالیت، اجزاء مولکولی مورد نظر و ماتریکس، سایراجزاء نمونه هستند. به منظور انجام HPLC، نمونه را به یک فاز متحرک وارد میکنند تا از میان فاز ساکن عبور کند. فاز متحرک را با شاخصههای مختلفی همچون ترکیب اجزا، انحلالپذیری، خواص فرابنفش، ویسکوزیته و امتزاج پذیری با سایر حلالها توصیف میکنند.
فاز ساکن میتواند تودهای از مایع متراکم، لایهای مایع بر سطحی جامد یا یک لایه بین سطحی (InterFacial)بین مایع و جامد باشد. در HPLC، فاز ساکن یک ماده دانهای با ذرات متخلخل بسیار کوچک در یک ستون جداسازی است. فاز متحرک، از طرف دیگر، یک حلال یا مخلوط حلال است که در فشار بالا از ستون عبور می کند. از طریق یک دریچه با یک حلقه نمونه متصل، یعنی یک لوله کوچک یا یک مویرگی ساخته شده از فولاد ضد زنگ، نمونه با استفاده از یک سرنگ به جریان فاز متحرک از پمپ به ستون تزریق می شود. متعاقباً، اجزاء منفرد نمونه با سرعتهای متفاوتی از طریق ستون مهاجرت میکنند، زیرا به درجات متفاوتی توسط برهمکنش با فاز ساکن حفظ میشوند. پس از خروج از ستون، مواد منفرد توسط یک آشکارساز مناسب شناسایی شده و به عنوان سیگنال به نرم افزار HPLC روی کامپیوتر ارسال میشود. در پایان این عملیات، کروماتوگرام در نرم افزارHPLC روی کامپیوتر به دست میآید. کروماتوگرام امکان شناسایی و تعیین کمیت مواد مختلف را فراهم می کند.
فاز ساکن به طور معمول به صورت یک ستون پرشده با اجزاءکوچک متخلخل است که فاز متحرک مایع، به کمک یک پمپ از میان آن عبور میکند. در حقیقت، توسعه HPLC با توسعه ستونهای جدید همراه بود که این امر نیازمند اجزاء جدید، فازهای ساکن جدید و دستورالعملهای بهبودیافته برای پرکردن ستون است.
اجزاء اصلی HPLC
مخزن حلال
پمپ
سیستم تزریق
ستون
آشکارساز
همان طور که در شکل زیر مشاهده میکنید، دستگاه کروماتوگرافی مایع با کارایی بالا شامل اجزاء زیر است:
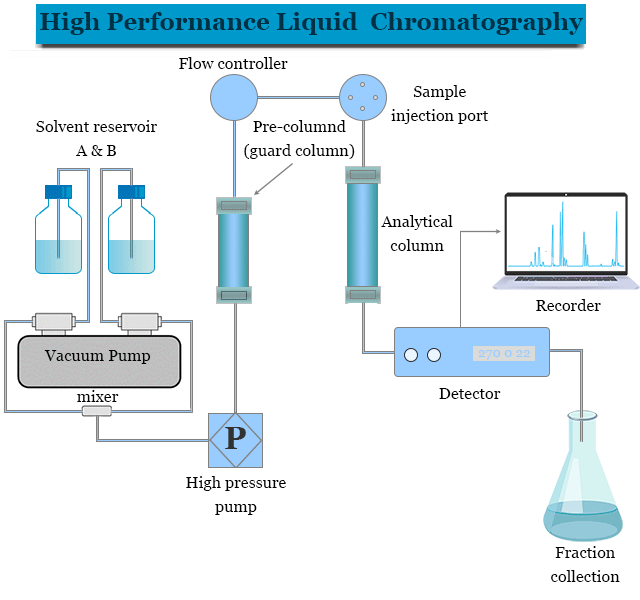
حلال
حلال ها در HPLC باید بسیار خالص باشند که بدین منظور از فیلترهای مخصوصی عبور داده میشوند، همچنین باید گاززدایی شوند تا حبابهای گاز محلول در آنها باعث اختلال در سیستم آشکارساز و پهنشدگی پیک نشوند. متداولترین حلالهای مورد استفاده، متانول، استونیتریل و آب هستند.
عبارت شویش در کروماتوگرافی به معنای عبور دادن اجزاء نمونه از میان ستون از طریق افزودن مداوم فاز متحرک است که به فاز متحرک اصطلاحاً شوینده میگویند. دو نوع شویش داریم:
- شویش ایزوکراتیک یا تک حلالی: در این روش، ترکیب حلال چه از نظر قطبیت و چه از نظر ماهیت در طی فرایند شویش تغییر نمیکند. استفاده از ایننوع سیستم حلال موجب افزایش زمان شویش شده و قدرت جداسازی گونههایی با قطبیت مشابه را ندارد. این روش زمانی مناسب است که اجزاء جداشونده دارای قطبیتهای به اندازه کافی متفاوت از یکدیگر باشند.
- شویش گرادیانی، شیبی یا چند حلالی: در این شویش از دو یا چند حلال با قطبیت مختلف استفاده می شود که نسبت آنها طبق برنامه زمانی تعیین شده تغییر میکند. در این روش قدرت شویش و جداسازی بالا رفته و در مخلوطهای پیچیده که اجزاء دارای گستره وسیعی از قطبیت هستند، امکان جداسازی بهتری را فراهم می کند. کوتاه شدنزمان جداسازی از دیگر مزایای این سیستم شویش است. این روش زمانی مناسب است که تعداد زیادی اجزاء با دامنه وسیعی از قطبیت وجود داشته باشند.
پمپ
کار پمپ آنچنان که از نامش پیداست، پمپاژ حلال و یا حلال ها با سرعت و جریان ثابت و فشار بسیار زیاد تا حدود ۴۰ مگا پاسکال یا بیشتر از میان فاز ساکن است. از مهمترین پمپها میتوان به پمپهای رفت و برگشتی یا پیستونی اشاره کرد. این واحد معمولا از یک تا چهار حلال را به سمت ستون پمپاژ می نماید که بسته به روشهای کاری تغییر میکند. در مواقعی که از یک حلال استفاده می شود به آن اصطلاحا ایزوکراتیک یا تک حلاله گفته میشود. در مواقعی نیاز هست تا از ترکیب ثابت دو یا چند حلال و یا ترکیب متغیر با زمان (برنامه زمانی) استفاده شود که به این سیستم باینری و یا کواترنری یا چند حلاله و یا گرادیانت می گویند. سیستم های باینری معمولا از سر هم بندی یا کوپلینگ دو پمپ همزمان ساخته می شوند و در مواقعی با استفاده از یک سیستم شیر چهار مسیره قابل کنترل با کامپیوتر که به ورودی پمپ متصل شده است می توان از ترکیب ثابت و یا متغیر با زمان همه حلال ها استفاده نمود.
سیستم تزریق
سیستم تزریق (Injector) در واقع نقش تزریق کننده نمونه به داخل حلال عبوری را بازی میکند. این سیستم متشکل از چند مسیر است که میتواند بین پمپ و ستون قرار گرفته و در حین عبور حلال یا فاز حامل با فشار زیاد، مقدار معینی از نمونه را به داخل آن هدایت نماید. مقدار ثابت نمونه در داخل لولهای با حجم مشخص به نام لوپ در کمین نشسته تا در لحظه فرمان کاربر، سوار موج حلال شده و به سمت ستون حرکت نماید.
بالا بودن فشار در سیستم به دلیل حضور پمپ ها، امکان تزریق مستقیم به دستگاه را غیرممکن میسازد. بر این اساس، سیستم تزریق شامل یک لوپ (حلقه نمونهبردار) با امکان بارگیری(Load) و تزریق (Inject) است. هنگام تزریق، انژکتور را روی لود قرار داده و سپس روی تزریق گذاشته تا نمونه تزریقی به سمت ستون حرکت کند. مقدار تزریق در HPLC کمتر از GC و در حدود ۵ تا ۵۰۰ ماکرولیتر است. همچنین در صورت داشتن تعداد نمونه بالا مخصوصاً در بخشهای تحقیقاتی از سیستم تزریق اتوماتیک (Autosampler) استفاده میشود. این سیستم میتواند تعداد بسیار زیادی از نمونه را طبق برنامه داده شده توسط کاربر به داخل حلال تزریق نماید.
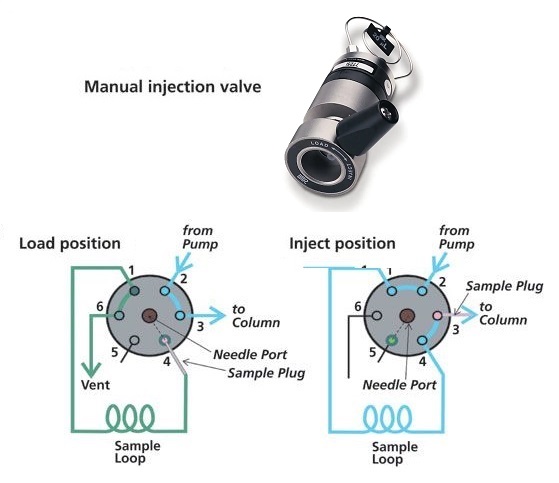
ستون
ستون (Column) مرکز جداسازی اجزاء نمونه در کروماتوگرافی مایع است. ستون HPLC لولهای است فلزی که با مواد نیمه تراوا از جنس خاک دیاتومه با خلل و فرج فراوان پر شده است و حلال و نمونه حل شده تنها با اعمال فشار از داخل آن عبور داده می شوند. کارایی این ستون ها به نگهداری و رها سازی مولکول های جزء به جزء ترکیب به ترتیب بزرگی و یا چسبندگی مولکول ها و قدرت شستشوی نمونه توسط حلال است. ستون ها بسته به جنس محتوا، قطبیت و طول دارای انواع متنوعی هستند که از متداول ترین آن ها ستون C18 و C8 می باشد.

فاز ساکن در ستون، اجزاء نمونه مورد نظر را از یکدیگر جدا میکند. حلال نمونه کمترین برهمکنش را با فاز ساکن دارد و زودتر از سایر ترکیبات به آشکارساز میرسد. ترکیبات دیگر نیز با توجه به میزان برهمکنش آنها با فاز ساکن که در بیشتر موارد بر اساس قطبیت آنها انجام میشود، در ستون جداسازی میشوند و هر کدام یک نوار (band) را در ستون تشکیل میدهند. هر دسته از این ترکیبات پس از خارج شدن از ستون و رسیدن به آشکارساز با یک پیک در کروماتوگرام نشان داده میشوند و ماهیت هر پیک با استفاده از زمانی که به آشکارساز میرسد مشخص میشود. همچنین میزان غلظت هر ترکیب با استفاده از اندازه سطح زیر پیک یا ارتفاع پیک قابل اندازهگیری است. گفتنی است زمان بازداری هر نمونه در صورت ثابت بودن تمامی پارامترها در جداسازی، ثابت بوده و با مقایسه آن با نمونه استاندارد، آنالیت مجهول قابل شناسایی و اندازهگیری کمی میباشد.
انواع ستون در HPLC
- ستونهای تجزیهای:این ستونها وظیفه اصلی جداسازی را بر عهده دارند. طول آنها ۵۰-۱۰ سانتیمتر و قطر داخلی ۱۰-۴ میلیمتر دارند. جنس آنها فولاد زنگ نزن بوده و قطر ذرات پرکننده در حدود چند میکرومتر است. ذرات پرکننده آن میتوانند ذرات لایهنشانی شده یا مواد متخلخل باشند.
- ستونهای محافظ (گارد):این ستونها تقریبا مشابه ستونهای تجزیهای بوده اما ذرات پرکننده آنها بسیار درشتتر و کوتاهتر میباشند. این ستونها قبل از ستون تجزیهای قرار گرفته و نقشی در جداسازی ندارند. به کارگیری آنها به دلایلی همچون حذف ناخالصی از حلال و آنالیت، اشباع کردن فاز متحرک از فاز ساکن و افزایش طول عمر ستون تجزیهای میباشد.
به طور کلی ستون ها به چند دسته تقسیم می شوند که در زیر به اختصار به توضیح آن ها می پردازیم:
ستون های فاز نرمال (Normal Phase)
در این نوع ستون ها، برهمکنش بین بخش های قطبی فاز ساکن و جسم حل شده وجود دارد. ترکیب فاز ساکن باید به نسبت فاز متحرک قطبی تر باشد.
ستون های فاز معکوس (Reversed Phase)
ماده موجود در این نوع ستون ها نسبتاً غیر قطبی و حلال قطبی است. برهمکنش بین ترکیبات غیر قطبی جسم های حل شده و فاز ساکن غیر قطبی رخ می دهد. این ستون ها در مقایسه با ستون های فاز نرمال زیست سازگارتر است.
ستون های تعویض یونی
ترکیبات نمونه در این نوع ستون ها که دارای دو نوع ستون کاتیونی (Cation Exchange) و ستون آنیونی (Anion Exchange) هستند، براساس نیروهای یونی بین مولکول های با بار مخالف نسبت به بارهای موجود در فاز ساکن، جدا می شوند.
ستون های اندازه طردی (طرد غربالی Size Exclusion)
در این ستون ها، مولکول ها براساس اندازه جدا میشوند. مولکول های کوچک به درون حفره های صافی نفوذ می کنند در حالی که مولکول های بزرگتر تنها به اندازه ای به درون آن ها نفوذ می کنند.
روشهای جداسازی در HPLC
بر اساس خواص فاز ساکن در ستون، از روش های جداسازی مختلفی استفاده میشود که از آن جمله میتوان به کروماتوگرافی فاز نرمال (Normal Phase Chromatography)، کروماتوگرافی فاز معکوس(Reverse Phase Chromatography)، کروماتوگرافی تبادل یونی(Ion Exchange Chromatography)، کروماتوگرافی اندازه طردی (Size Exclusion Chromatography) و کروماتوگرافی میل ترکیبی (Affinity Chromatography) اشاره کرد.
کروماتوگرافی فاز نرمال
در این روش، ستون را با ذرات قطبی معدنی پر و از یک فاز متحرک ناقطبی برای عبور از میان فاز قطبی استفاده میکنند. از کروماتوگرافی فاز نرمال به طور عمده برای خالصسازی نمونههای خام، جداسازی نمونههای به شدت قطبی یا جداسازی تحلیلی با کروماتوگرافی لایه نازک بهره میگیرند. یکی از مشکلات استفاده از این روش این است که آب، حلالی قوی برای کروماتوگرافی فاز نرمال به شمار میآید و وجود آب در فاز متحرک به طور محسوسی بر بازداری نمونه تاثیر گذار است. در جدول زیر، نوع فازهای متحرک و ساکن در کروماتوگرافی فاز نرمال و معکوس آورده شده است.
کروماتوگرافی فاز معکوس
در کروماتوگرافی فاز معکوس، فاز ساکن، دارای خاصیت آبگریز (Hydrophobic) است درحالی که فاز متحرک خاصیتی قطبی دارد. همان طور که در جدول بالا نیز نشان داده شده است، نوع قطبیت فازها، عکس کروماتوگرافی فاز نرمال می باشد. نوع برهمکنشها درHPLC با فاز معکوس (RP-HPLC) را به صورت نیروهای آبگریز در نظر میگیرند. این نیروها نتیجه انرژی حاصل از تغییر در ساختارهای دوقطبی حلال است. جدایش مواد به طور عمده ناشی از تقسیم شدن آنالیت بین فاز ساکن و متحرک ذکر میشود.
مولکولهای حلشونده در تعادل بین فاز ساکن آبگریز و فاز متحرک با قطبیت جزئی هستند. هر قدر مولکول آبگریز (غیرقطبی) باشد، زمان بازداری طولانیتری خواهد داشت درحالی که ترکیبات معدنی یونیزه شده، یونهای معدنی و مولکولهای فلزی قطبی، زمان بازداری کمی دارند.
کروماتوگرافی تبادل یونی
مکانیسم تبادل یونی، بر اساس برهمکنش الکترواستاتیک بین یونهای آبدار از نمونه و گروههای عاملی با بار مخالف فاز ساکن بنا شده است. دو مکانیسم برای جداسازی مورد استفاده قرار میگیرد. در یک مکانیسم، به هنگام شویش، از فاز متحرک با یونهایی استفاده می شود که با یونهای آنالیت جایگزین شوند و این یونها را به خارج از ستون هدایت میکنند.
مکانیسم دیگر، شامل اضافه کردن ریجنت کمپلکس کننده به فاز ساکن برای تغییراجزاء نمونه از حالت اولیه خود است. با انجام چنین فرآیندی روی مولکولها، عمل شویش انجام میشود. علاوه بر تبادل یونها، تبادل یونی فاز ساکن میتواند برخی از مولکولها را به صورت خنثی نگه دارد. این فرآیند با میزان بازداری در تشکیل کمپلکسها مرتبط میشود. یونهای ویژهای همچون فلزات واسطه میتوانند بر رزینهای تبادل کاتیونی قرار بگیرند و با پذیرفتن جفت الکترونهای ناپیوندی، لیگاندهای دهنده (Donor) را بپذیرند.
کروماتوگرافیهای تبادل یونی امروزی، امکان تحلیلهای مقداری در غلظتهای پایین حلشونده را دارند. از آنها میتوان به منظور آنالیز نمونههای محلول در آب آنیونهای معدنی استفاده کرد. کاتیونهای فلزی و آنیونهای معدنی به طور عمده توسط برهمکنشهای یونی با رزینهای تبادل یونی، از یکدیگر جدا میشوند.
یکی از کاربردهای صنعتی کروماتوگرافی تبادل یونی در صنایع غذایی است که برای تعیین اجزاء شامل نیتروژن، گوگرد، فسفر و یونهای هالید از آن بهره میگیرند. همچنین، این روش میتواند برای تعیین یونهای معدنی و آلی در آبها استفاده شود.
کروماتوگرافی اندازه طردی
کروماتوگرافی اندازه طردی(Size Exclusion Chromatography)، روشی برای جداسازی مولکولها بر اساس اندازه است. از این روش به طور معمول برای جداسازی درشت مولکولها از مولکولهای کوچکتر استفاده میشود. بعد از تزریق آنالیت به ستون، مولکولهایی که از اندازه حفرات فاز ساکن کوچکتر باشند، به داخل ذرات متخلخل وارد میشوند در بین کانالهای تودرتوی فاز ساکن جریان پیدا میکنند اما مولکولهای بزرگتر باید مسیر طولانیتری را برای خروج طی کنند و در نتیجه، دیرتر از ستون خارج میشوند.
با توجه به اینکه حجم مولکولی با جرم مولکولی مرتبط است، انتظار میرود که زمان بازداری، به نحوی با جرم مولکولی مواد پلیمری مرتبط باشد. ارتباط بین زمان بازداری و جرم مولکولی در تصویر زیر نشان داده شده است:
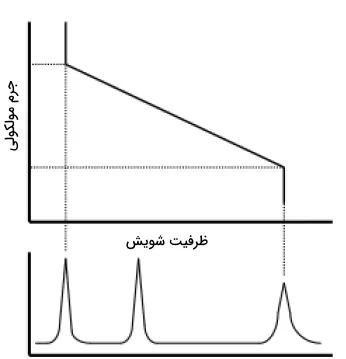
به طور معمول، نوع HPLC به طبیعت شیمیایی و پارامترهای فیزیکوشیمیایی نمونه بستگی دارد. در تصویر زیر، فلوچارتی برای تعیین روش HPLC نمایش داده شده است.
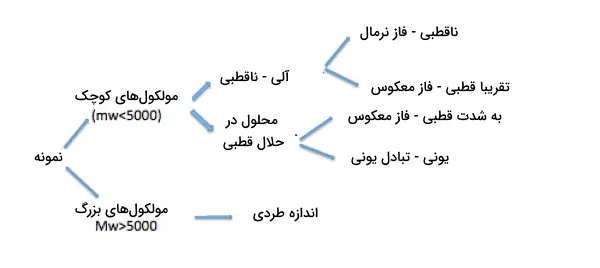
بخاری ستونی (Column Heater)
جداسازی LC اغلب تا حد زیادی تحت تأثیر دمای ستون است. برای به دست آوردن نتایج قابل تکرار، حفظ شرایط دمایی ثابت مهم است. همچنین برای برخی از تجزیه و تحلیل ها، مانند قند و اسید آلی، وضوح بهتری را می توان در دماهای بالا (۵۰ تا ۸۰ درجه سانتی گراد) به دست آورد. بنابراین ستون ها به طور کلی در داخل کوره ستونی (هیتر ستونی) نگهداری می شوند.
گازگیر (Degasser)
حلال مورد استفاده برای تجزیه و تحلیل LC ممکن است حاوی گازهایی مانند اکسیژن باشد که برای چشم ما قابل مشاهده نیست. هنگامی که گاز در حلال وجود دارد، این به عنوان نویز تشخیص داده می شود و باعث ایجاد خط پایه ناپایدار می شود. بنابراین حلال قبل از ورود به پمپ باید عاری از هرگونه حباب هوا و یا گاز و هوای حل شده در آن باشد. این کار به روش تزریق گاز بیاثر مثل آرگون به داخل حلال در حین لرزاندن و یا استفاده از دستگاه گازگیر صورت میگیرد. اگرچه امروزه درHPLC بیشتر از دستگاه Degasser استفاده میشود و سیستم نیمه تراوای داخل آن گاز را تراوش نموده ولی اجازه خروج مایع را نمیدهد. گاز زدا از لوله های غشایی پلیمری مخصوص برای حذف گازها استفاده می کند. منافذ بسیار کوچک روی سطح لوله پلیمری به هوا اجازه عبور می دهد و در عین حال از عبور مایع از منافذ جلوگیری می کند.
آشکارساز
آشکارساز دستگاهی است که میتواند غلظت نمونه در دستگاه کروماتوگرافی مایع را بر اساس خاصیتی مثل میزان جذب بسنجد. دتکتور دستگاه کروماتوگراف غالباً یک اسپکتروفتومتر است که مقدار و نوع نمونه را در طول موج خاصی نمایش میدهد و این دتکتور SPD نامیده میشود. دتکتورRID از دیگر دتکتورهای مرتبط است که نمونه را بر اساس ضریب شکست آن شناسائی و مقدارسنجی میکند، دتکتورRF هم نمونه را براساس میزان فلورسانس و دتکتور MS نمونه را براساس جرم مولکولی شناسایی و مقدار سنجی میکنند.
نمونه بعد از جداسازی در ستون وارد آشکارساز شده و با دریافت هر جزء ازاجزاء نمونه یک سیگنال الکتریکی تولید میکند که پس از ارسال به یک دستگاه رسام، کروماتوگرام نمونه رسم میشود. شدت هر پیک مربوط به هر ترکیب با مقدار کمی آن جزء متناسب است. از نظر تئوری یک آشکارساز زمانی در شرایط ایدهآل و بهینه قراردارد که بتواند تمام اجزاء نمونه را به محض خروج از ستون تشخیص داده و متناسب با غلظت هر جزء یک سیگنال تولید کند. پس سرعت پاسخگویی و حساسیت یک آشکارساز مهمترین خصوصیت آن میباشد.
آشکارسازها در کروماتوگرافی HPLC
آشکارسازهایی که در کروماتوگرافی مایع مورد استفاده قرار میگیرند، بیشتر شامل آشکارسازیهای ماورای بنفش- مرئی هستند. شاخصههای اساسی آشکارسازها در کروماتوگرافی مایع عبارتند از:
- گستره دینامیکی (Dynamic Range)
- شاخص پاسخ (Response Index)
- گسترده دینامیکی خطی
- پاسخ آشکارساز
- حساسیت
در میان این آشکارسازها، معروفترین و اقتصادیترین روش، استفاده از آشکارسازهای ماورای بنفش (UV) و ضریب شکست نور (RI) است. این آشکارسازها محدوده شناسایی منطقی گستردهای دارند.
آشکارسازهای UV-VIS یا PDA
آشکارسازهای UV-VISاز رایج ترین آشکارسازهای HPLC و جزو آشکارسازهای جذبی هستند که حساسیت خوبی برای ترکیبات جاذب نور دارند. در هنگام آنالیز، نمونه وارد یک سل شیشهای بی رنگ، به نام Flow cell می شود. هنگامی که نور UV بر سل جریان تابش میشود، نمونه بخشی از نور UV را جذب می کند. شدت نور UV برای فاز متحرک بدون نمونه (شاهد) و حاوی نمونه متفاوت خواهد بود. با اندازه گیری این تفاوت، مقدار نمونه تعیین می شود. از آنجایی که این دتکتور با استفاده از قانون بیر لامبرت کار می کند لازم است که برای هر آنالیت طول موج مناسب را انتخاب نمود. یک دتکتور UV در طول موج بین ۱۹۵تا ۳۷۰ نانومتر اندازه گیری می کند که بیشترین استفاده در ۲۵۴ نانومتر است. در مقایسه با یک آشکارسازUV، آشکارساز VIS گستره بیشتری (۴۰۰ تا ۷۰۰ نانومتر) دارد.
آشکار سازهای فتودیود آرای توانایی جمع آوری همزمان چندین طول موج در یک آنالیز و همچنین مقایسه داده های طیفی ترکیبات باهم را دارند. آشکارسازهای UV و VIS نتایج به دست آمده را در دو بعد شدت نور و زمان نشان می دهند اما PDA بعد سوم یعنی طول موج را نیزاضافه می کند.
آشکارسازهای ماورای بنفش تنها برای موادی کاربرد دارند که نور ماورای بنفش را در طول موج منبع نوری جذب میکنند. لازم به ذکر است که بسیاری از ترکیبات، نور را در دامنه ماورای بنفش (۳۵۰-۱۸۰ نانومتر) جذب میکنند که از آن جمله میتوان به مواد پیوندهای یگانه یا موادی با الکترون غیراشتراکی اشاره کرد.
از آشکارسازهای ماورای بنفش به طور مؤثر در کروماتوگرافی فاز معکوس و تبادل یونی بهره میگیرند. آشکارسازهای ماورای بنفش، حساسیت بالا و قیمت مناسبی دارند و کار کردن با آنها ساده است. به همین دلیل، آشکارسازهای ماورای بنفش، بیشترین استفاده رHPLC دارند.
آشکارساز (RI) Reflactive Index
آشکارساز RI تغییر در شاخص رفلکس را اندازه گیری می کند. سل شیشه ای به دو سل تقسیم می شود. خروجی از ستون وارد سل نمونه شده و سل دیگر(سل مرجع) تنها با فاز متحرک پر شده است. هنگامی که جریان خروجی وارد سل نمونه که حاوی هیچ آنالیتی نیست می شود، حلال در داخل هر دو سلول یکسان است.
(A) هنگامی که یک پرتو بر روی سل ها تابیده می شود، پرتو مشاهده شده در این مورد مستقیم خواهد بود.زمانی که خروجی ستون دستگاه HPLC حاوی ترکیب دیگری به غیر از فاز متحرک باشد پرتو ورودی به دلیل اختلاف شاخص رفلکس بین دو حلال خم می شود.
(B) با اندازه گیری این تغییر، حضور اجزاء مشاهده می شود.
به طور کلی از این آشکارساز برای ترکیباتی نظیر شکر،الکل ها،یون های معدنی و هیدروکربن ها که در UV جذب ندارد استفاده می شود و حساسیت آن نسبت به UV کمتر است.
آشکارسازهای RI از اولین آشکارسازهای تجاری بودند که مورد استفاده قرار گرفتند. این روش به طور ویژه در HPLC بر اساس اندازه کاربرد دارد و اندازهگیری آن به طور مستقیم به غلظت پلیمر وابسته و مستقل از جرم مولکولی است.
آشکار ساز پراکندگی نور (ELSD) Evaporative Light Scattering Detector
آشکار ساز پراکندگی نور حساسیت خوبی برای آنالیت های غیرفرار در مقیاس نانوگرم (ng) دارد.به طور کلی این دتکتور، برای ترکیباتی که فراریت کمتری نسبت به فاز متحرک دارند و همچنین ترکیباتی که قادر به جذب نورUV نیستند مانند قندها، آنتی بیوتیکها، اسیدهای چرب، چربیها، روغنها، فسفولیپیدها، پلیمرها و تری گلیسیریدها استفاده می شود. طریقه کارایی این دتکتور به این صورت است که خروجی ستون HPLC اسپری شده و سپس فاز متحرک تبخیر می گردد تا ذرات ریزی را ایجاد کند، سپس نور لیزر به آنالیت تابیده می شود و بازتابش پراکنده شده آن توسط دتکتور تشخیص داده می شود. کارایی ELSD تقریبا مشابه RI است اما نسبت به آن حساس تر است.
آشکارساز الکتروشیمیایی (EC)
بر اساس اندازه گیری جریان حاصل از واکنش اکسیداسیون/احیای آنالیت در الکترود مناسب استوار است و تشخیص برر اساس روش های الکتروشیمیایی نظیر پلاروگرافی،کولومتری،آمپرومتری و هدایت سنجی می باشد.
آشکارساز پخش نور چند زاویه ای Multi-Angle Light Scattering Detector (MALS)
در آنالیز Size exclusion chromatography (SEC) یا غربالگری، جرم ملکولی آنالیت از روی نمودار کالیبراسیون و با استفاده از محلول استاندارد تعیین می شود. در حالی که با استفاده از دتکتور پخش نور چند زاویه ای، جرم ملکولی به طور مستقیم و بدون نیاز به منحنی کالیبراسیون تعیین می گردد. علاوه بر آن با استفاده از دتکتور MALS در کروماتوگرافی مایع با کارایی بالا می توان جرم ملکولی مطلق آنالیت را با حد تشخیص بسیار پایین تعیین کرد.
آشکارساز طیف سنجی جرمی Mass Spectroscopy
روش دیگری موسوم به طیفسنجی جرمی، مزایایی خاصی نسبت به سایر روشها دارد. طیف جرمی را میتوان به سرعت به دست آورد و تنها مقادیر کمی از ماده برای نمونهگیری و تحلیل لازم است. علاوه بر این، دادهای که از این روش به دست میآید، اطلاعات مفیدی را در خصوص ساختار مولکول در اختیار ما قرار میدهد. از ترکیب کروماتوگرافی HPLC و طیفسنج جرمی به منظور شناسایی ویژه و تعیین مواد شیمیایی استفاده میشود. ذکر این نکته لازم است که ترکیب کروماتوگرافی مایع با طیفسنج جرمی قدری دشوار است چراکه در ابتدا باید تمامی حلال خارج شود.
بر اساس وزن مولکولی آنالیت شناسایی می شوند.به طور کلی برای ترکیبات پایدار حرارتی،قطبی و با وزن مولکولی بالا استفاده می گردند.
آشکارساز هدایت الکتریکی Conductivity Detector
دتکتور CD در کروماتوگرافی یونی استفاده می شود و برای محلول های حاویاجزاءیونی کاربرد دارد.مقاومت الکترونیکی توسط دتکتور اندازه گیری می شود که این عدد متناسب با غلظت یون های موجود در محلول است.
آشکارساز چرخش نوری Optical Rotation Detector
دتکتور OR برای اندازه گیری ترکیبات دارای ایزومر نوری استفاده می شود و قادر به جداسازی ایزومرهای نوری R وL می باشد.
آشکارساز رزونانس مغناطیس هسته
اتصال روش های جداسازی کروماتوگرافی با NMR منجر به ایجاد روشی قدرتمند و سریع برای جداسازی و تبیین ساختاری ترکیبات مجهول و مخلوط ها شده است. حساسیت پایین این روش با مزایای فراوانی که در پی دارد جبران می شود.
آشکارساز فلورسانس Fluorescence Detector (FL)
در دتکتورهای فلورسانس با استفاده از یک طول موج خاص، اتم های آنالیت برانگیخته شده و از خود یک نور تک پرتویی منتشر می کنند. شدت نور فلورسانس منتشر شده برای اندازه گیری غلظت آنالیت به کار برده می شود. بسیاری از داروها، محصولات طبیعی، نمونه های پزشکی و محصولات پتروشیمی دارای جذب فلورسانس می باشند. برای سایر مواد که جذب فلورسانس ندارند یا جذب پایینی دارند می توان از مشتقات فلورسانس مانند دانسیل کلرید استفاده کرد.
آشکارساز نورتابی شیمیایی Chemiluminescence Detector (CLD)
دتکتور نورتابی شیمیایی مشابه FLمی باشد اما به جای استفاده از منبع نور برای برانگیخته کردن اتم ها، برانگیختگی در ابتدا توسط واکنش شیمیایی انجام می شود. از آنجا که استفاده از دتکتور CLD بر روی دستگاه HPLC وابسته به منبع برانگیختگی خارجی نیست، نویز دتکتور بسیار کم است که باعث افزایش حساسیت و دقت آن نسبت به دتکتور FL می شود.
نانوفناوری در کروماتوگرافی مایع با کارایی بالا
معرفی نانومواد به عنوان فاز ساکن در کروماتوگرافی مایع به دلیل سطح و خصوصیات ساختاری این دسته از مواد در کنار توانایی آنها در برقراری برهمکنش خاص با آنالیتها، مزایای بیشماری در این زمینه ایجاد کرده است. نانو مواد منشأ پیشرفتهای مهمی در زمینه کارایی، گزینش پذیری و افزایش رزولوشن و همچنین توسعه بیشتر سیستمهای کوچک مینیاتوری و باعث کاهش مصرف حلال و سادهسازی پروسه جداسازی شدهاند.
بر اساس آمادهسازی فاز ساکن، دو دیدگاه وجود دارد. از یک سو بسیاری از محققان توجه خود را به تهیه ستونهایی متمرکز کردهاند که در آن به دلیل آمادهسازی همزمان، نفوذپذیری زیاد، شیمی سطح گسترده در دسترس و خاصیت تخلخل خوب؛ نانومواد به ماده دیگری که به عنوان تکیهگاه استفاده میشود (معمولا ذرات ریز سیلیکا یا پوششهای یکپارچه پلیمری)، متصل میشوند. از طرفی دیگر، (اگرچه کمتر مورد استفاده قرار میگیرد) نانومواد جزء اصلی فاز ساکن بدون هیچگونه اصلاح سطح بوده و به عنوان پوششی برای اجزاء خاص عمل میکنند. در هر دو مورد، نوع نانومواد مورد استفاده، بسیار متنوع هستند. بدین منظور، نانو مواد آلی و معدنی یا انواع مواد کربنی مانند نانولوله کربنی، گرافن و فولرین در میان دیگر مواد به دلیل کاربرد مناسب آنها به عنوان فاز ساکن در کروماتوگرافی ارزیابی شدند.
کاربرد کروماتوگرافی مایع با کارایی بالا در آنالیز نانومواد
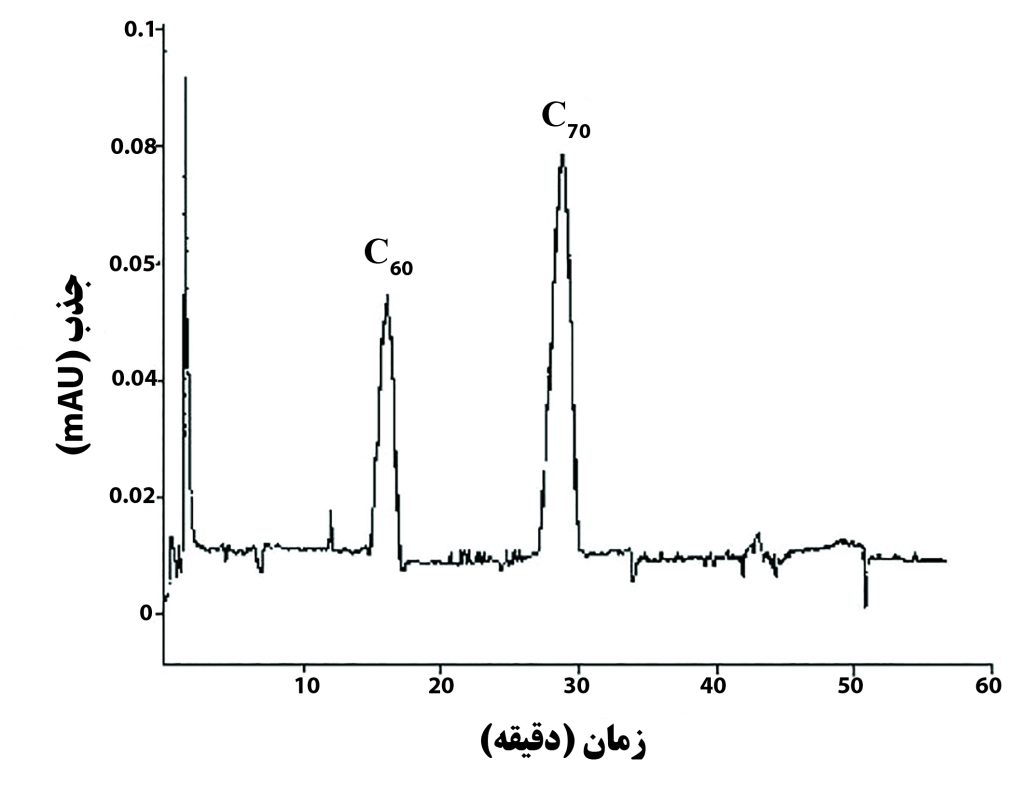
روش HPLC در آنالیز نانو مواد نیز کاربرد دارد. همانطور که در شکل ۹ مشاهده میکنید، برای شناسایی فولرن 60C و 70C از اتصال (کوپل شدن) HPLC با دیگر روشهای آنالیز (FT-IR)؛ بر اساس برنامه شویش ایزوکراتیک با ستون غیرقطبی C18 و مخلوط استونیتریل-تولوئن (۱:۱) به عنوان فاز متحرک استفاده شده است. با داشتن زمان خروج نمونه استاندارد و مقایسه آن با زمان خروج نمونه از ستون میتوان شناسایی کیفی را انجام داد و همچنین با بدست آوردن سطح زیر پیک، غلظت نمونه را میتوان اندازه گیری کرد (شناسایی کمی).
منابع : سهیل بهر کاظمی- حانیه نورمحمدی- کیمیا زیست گستر نوین







